Содержание:
В силикат кальция это название, данное группе химических соединений, образованных оксидом кальция (CaO) и кремнеземом (SiO2). Общая формула этих соединений: xCaO • ySiO2• zH2ИЛИ.
Это белые или желтовато-белые твердые вещества. Они могут быть безводными, то есть без воды (H2O) в своей структуре или может содержать его. В природе они входят в состав нескольких видов минералов.

Силикаты кальция нерастворимы в воде, но когда они соединяются с ней, они образуют гидратированные гели (такие материалы, как желатин), которые очень твердые, устойчивые и почти водонепроницаемые при застывании.
Это привело к их использованию в строительной отрасли, так как они используются в цементе, кирпиче и влагоизоляционных панелях. Они также являются частью материалов для заживления перфораций в зубах и даже были изучены для использования при регенерации костей, то есть в качестве биоматериала.
Они были предложены для уменьшения загрязнения, создаваемого некоторыми металлургическими предприятиями. Они также используются в качестве генераторов трения в тормозах и сцеплениях транспортных средств.
Свойства
Физические свойства
Металл кальций существует в двух аллотропных модификациях. До 443 °C устойчив α-Ca с кубической гранецентрированной решеткой (параметр а = 0,558 нм), выше устойчив β-Ca с кубической объемно-центрированной решеткой типа α-Fe (параметр a = 0,448 нм). Стандартная энтальпия ΔH
0 перехода α → β составляет 0,93 кДж/моль.
Химические свойства
Кальций — типичный щелочноземельный металл. Химическая активность кальция высока, но ниже, чем всех других щелочноземельных металлов. Он легко взаимодействует с кислородом, углекислым газом и влагой воздуха, из-за чего поверхность металлического кальция обычно тускло серая, поэтому в лаборатории кальций обычно хранят, как и другие щелочноземельные металлы, в плотно закрытой банке под слоем керосина или жидкого парафина.
В ряду стандартных потенциалов кальций расположен слева от водорода. Стандартный электродный потенциал пары Ca2+/Ca0 −2,84 В, так что кальций активно реагирует с водой, но без воспламенения:
С активными неметаллами (кислородом, хлором, бромом) кальций реагирует при обычных условиях:
2Са + О2 = 2СаО, Са + Br2 = CaBr2.
При нагревании на воздухе или в кислороде кальций воспламеняется. С менее активными неметаллами (водородом, бором, углеродом, кремнием, азотом, фосфором и другими) кальций вступает во взаимодействие при нагревании, например:
Са + Н2 = СаН2, Ca + 6B = CaB6,
3Ca + N2 = Ca3N2, Са + 2С = СаС2,
3Са + 2Р = Са3Р2 (фосфид кальция), известны также фосфиды кальция составов СаР и СаР5;
2Ca + Si = Ca2Si (силицид кальция), известны также силициды кальция составов CaSi, Ca3Si4 и CaSi2.
Протекание указанных выше реакций, как правило, сопровождается выделением большого количества теплоты (то есть эти реакции — экзотермические). Во всех соединениях с неметаллами степень окисления кальция +2. Большинство из соединений кальция с неметаллами легко разлагается водой, например:
Ион Ca2+ бесцветен. При внесении в пламя растворимых солей кальция пламя окрашивается в кирпично-красный цвет.
Такие соли кальция, как хлорид CaCl2, бромид CaBr2, иодид CaI2 и нитрат Ca(NO3)2, хорошо растворимы в воде. Нерастворимы в воде фторид CaF2, карбонат CaCO3, сульфат CaSO4, ортофосфат Ca3(PO4)2, оксалат СаС2О4 и некоторые другие.
Важное значение имеет то обстоятельство, что, в отличие от карбоната кальция СаСО3, кислый карбонат кальция (гидрокарбонат) Са(НСО3)2 в воде растворим. В природе это приводит к следующим процессам
Когда холодная дождевая или речная вода, насыщенная углекислым газом, проникает под землю и попадает на известняки, то наблюдается их растворение:
СаСО3 + СО2 + Н2О = Са(НСО3)2.
В тех же местах, где вода, насыщенная гидрокарбонатом кальция, выходит на поверхность земли и нагревается солнечными лучами, протекает обратная реакция:
Так в природе происходит перенос больших масс веществ. В результате под землей могут образоваться огромные провалы, а в пещерах образуются красивые каменные «сосульки» — сталактиты и сталагмиты.
Наличие в воде растворенного гидрокарбоната кальция во многом определяет временную жёсткость воды. Временной её называют потому, что при кипячении воды гидрокарбонат разлагается, и в осадок выпадает СаСО3. Это явление приводит, например, к тому, что в чайнике со временем образуется накипь.
Кальций содержащие препараты
Есть много вариантов, при помощи которых возможно восполнить недостающую норму элемента в организме. Лучше всего, конечно, естественные методы — продукты, содержащие нужный атом. Однако если это по каким-либо причинам недостаточно или невозможно, медицинский путь также приемлем.
Так, список продуктов, содержащих кальций, примерно такой:
- молочные и кисломолочные изделия;
- рыба;
- зелень;
- зерновые культуры (гречка, рис, выпечка из цельнозерновой муки);
- некоторые цитрусовые (апельсины, мандарины);
- бобовые;
- все орехи (особенно, миндаль и грецкие).
Если же на какие-то продукты аллергия или нельзя употреблять их по другой причине, то восполнить уровень нужного элемента в организме помогут кальций содержащие препараты.

Все они представляют собой соли этого металла, обладающие способностью легко усваиваться организмом, быстро всасываясь в кровь и кишечник. Среди них самыми популярными и используемыми являются следующие.
- Хлорид кальция — раствор для инъекций или для приема внутрь взрослым и детям. Отличается концентрацией соли в составе, используется для «горячих уколов», поскольку вызывает именно такое ощущение при вкалывании. Есть формы с фруктовым соком для облегчения приема внутрь.
- Глюконат кальция. Выпускается как таблетками (0,25 или 0,5 г), так и растворами для внутривенных инъекций. Часто в виде таблеток содержит различные фруктовые добавки.
- Лактат кальция — выпускается в таблетках по 0,5 г.
https://youtube.com/watch?v=n19F3XTqjDU
Свойства кальция
Кальций — элемент IIA группы периодической системы, его содержание в земной коре составляет 3,6%. Кальций — один из самых химически активных металлов, имеет следующие физико-химические свойства: атомная масса 40,08; валентность 2; плотность 1,54 г/см3; температура плавления 810° С, кипения 1439° С.
С кислородом кальций дает исключительно прочное соединение — оксид CaO, теплота образования которого 626 кДж/моль (151 790 кал/моль), температура плавления 2587° С, кипения 3627° С. С углеродом кальций образует прочный карбид CaC2 с температурой плавления 2300° С. С кремнием кальций образует три силицида Ca2Si, CaSi и CaSi2. Кальций и железо взаимно нерастворимы. Вместе с тем в жидком состоянии и железо, и кальций в отдельности неограничено растворяются кремнием
Кальций в виде сплава с кремнием, (СК25 и СКЗО) или в виде тройного сплава (СК10, СК15) широко используют для раскисления стали, а также для производства ряда комплексных сплавов и модификаторов. Состав силикокальция приведен в табл. 21.
В биоматериалах
Керамика из силиката кальция начала испытываться в качестве биоматериала с 1990 года. Ее изучали на предмет их потенциального использования в регенерации костной ткани, поскольку они обладают более высокой биологической активностью, чем другие материалы.
Это связано с тем, что они содержат кремний (Si), который играет важную роль в механизмах, которые приводят к образованию новой кости.
Цементы на основе силиката кальция обладают способностью вызывать образование покрытия из фосфата / апатита кальция при погружении в биологические жидкости и способствовать регенерации тканей.
По этим причинам он считается подходящим материалом для восстановления костей.
Применение Кальция
Применение такого химического элемента как кальций относительное. С одной стороны применение чистого кальция довольно ограничено, а с другой стороны кальциевые соединения применяются почти во всех сферах жизнедеятельности. Наибольшее использование чистого кальция приходится на литейную промышленность благодаря его сильному химическому родству к кислороду и сере. В конкретных случаях, он применяется в качестве добавки при производстве стали, а так же в качестве восстановителя при производстве таких металлов ка торий, цирконий, ванадия, хрома и урана. Он также может использоваться для хранения газообразного водорода, так как он реагирует с водородом с образованием твердого гидрида кальция. Из этого соединения водород извлекается без особого труда и затрат.
Конечно с самого начала следует отметить роль кальциевых соединений в сторительной промышленности. Такие вещества как известь, гипс и мрамор используются повсеместно. Ионы кальция могут применяться в автомобильных необслуживаемых аккумуляторах. В этих аккумуляторах он уменьшает снижение потерь воды и саморазряда. Химическая промышленность добавляет ионы кальция в некоторые очистители сточных вод, моющие и дезинфицирующие средства, зубные пасты и многое другое. Роль кальция в пищевой промышленности почти полностью посвящается пищевым добавкам из-за благоприятного воздействия на организм человека.
Это утверждение можно связать и с медициной, так как кальций укрепляет(восстанавливает) кости и играет роль в синтезе белков. Поэтому разработано очень много медицинских препаратов предназначенных для восстановления баланса кальция в организме человека. У соединений кальция очень широкий круг применения начиная от школьного мела и заканчивая наполнителями пластмасс, металлическим мылом и синтетических смол.
Читайте: Сера как химический элемент таблицы Менделеева
[править] Химические свойства
Реакция кальция с водой Кальций относится к главной подгруппе второй группы периодической системы Менделеева. Его атомы на внешнем энергетическом уровне имеют по два электрона. Эти электроны он легко теряет и превращается в положительно заряженные ионы Са2+. Во всех своих соединениях кальций бывает только двухвалентный. Кальций принадлежит к самым активным металлов и по своей химической активности уступает лишь щелочным металлам.
При обычной температуре кальций легко взаимодействует с кислородом и влагой воздуха, поэтому его хранят под слоем керосина, вазелина или в герметически закрытом сосуде. При нагревании он легко воспламеняется, образуя оксид кальция:
Кальций легко взаимодействует также с водой, особенно при нагревании, а с кислотами реагирует очень бурно:
С влажным бромом и хлором кальций взаимодействует уже при обычной температуре, а при нагревании непосредственно реагирует с серой, азотом, графитом и другими веществами, а также восстанавливает почти все металлы из их оксидов:
Кальциевая селитра
Водорастворимое удобрение с высоким содержанием азота (13-15%) и доступного кальция (19-27%). Химическая формула — Са(NО3)2, внешне — белый порошок без вкуса, цвета и запаха, хорошо растворимый в воде.
Кальциевая селитра — щелочное удобрение, пригодное для ВСЕХ почв и прежде всего для кислых.
Когда лучше вносить кальциевую селитру?
Кальциевую селитру можно вносить в течение всего вегетационного периода с поливом и в сухом виде. Применяет в основном как азотное удобрение, считается наиболее эффетивным для весенней подкормки озимых культур.
Кальциевую селитру не вносят по осени, под перекопку или вспашку. Т.к. при осенней закладке произойдет распад удобрения с выделением азота. А без азота кальций не будет усваиваться растениями, а значит польза удобрения будет сведена к минимуму.
Особенности кальцинита
Нормы расхода кальцинита при корневым подкормках:
- Клубника, или садовая земляника – 25 г / 10 л. Подкормку проводят строго до начала цветения.
- Овощи (толерантные к кальцию) – 20 г / 10 л. Подкормку проводят до цветения.
- Плодовые деревья (яблони, груши), кустарники – 25-30 г / 10 л. Подкормку проводят до распускания почек.
- Внекорневые подкормки кальционитом — 1-2 г / 1 л воды (1-2 кг на 100 л).
Кальционит нельзя мешать с другими удобрениями, его вносят отдельно.
Нельзя смешивать кальциевую селитру с удобрениями, содержащими фосфаты и сульфаты, ввиду выпадения в нерастворимый осадок элементов питания. По этой причине, кальций, как правило, не входит в состав комплексных удобрений.
Также, кальциевую селитру нельзя вносить одновременно с пестицидами, гербицидами и стимуляторами роста.
Нахождение в природе
Из-за высокой химической активности кальций в свободном виде в природе не встречается.
На долю кальция приходится 3,38 % массы земной коры (5-е место по распространенности (3-е среди металлов) после кислорода, кремния, алюминия и железа). Содержание элемента в морской воде — 400 мг/л.
Изотопы
Основная статья: Изотопы кальция
Кальций встречается в природе в виде смеси шести изотопов: 40Ca, 42Ca, 43Ca, 44Ca, 46Ca и 48Ca, среди которых наиболее распространённый — 40Ca — составляет 96,97 %. Ядра кальция содержат магическое число протонов: Z = 20. Изотопы 40 20Ca20 и 4820Ca28 являются двумя из пяти существующих в природе дважды магических ядер.
Из шести природных изотопов кальция пять стабильны. Шестой изотоп 48Ca, самый тяжёлый из шести и весьма редкий (его изотопная распространённость равна всего 0,187 %), испытывает двойной бета-распад с периодом полураспада (4,39 ± 0,58)⋅1019 лет.
В горных породах и минералах
Кальций, энергично мигрирующий в земной коре и накапливающийся в различных геохимических системах, образует 385 минералов (четвёртое место по числу минералов).
Большая часть кальция содержится в составе силикатов и алюмосиликатов различных горных пород (граниты, гнейсы и т. п.), особенно в полевом шпате — анортите Ca[Al2Si2O8].
Кальцит
Довольно широко распространены такие минералы кальция, как кальцит CaCO3, ангидрит CaSO4, алебастр CaSO4·0.5H2O и гипс CaSO4·2H2O, флюорит CaF2, апатиты Ca5(PO4)3(F,Cl,OH), доломит MgCO3·CaCO3. Присутствием солей кальция и магния в природной воде определяется её жёсткость.
Осадочная порода, состоящая в основном из скрытокристаллического кальцита — известняк (одна из его разновидностей — мел). Под действием регионального метаморфизма известняк преобразуется в мрамор.
Миграция в земной коре
В естественной миграции кальция существенную роль играет «карбонатное равновесие», связанное с обратимой реакцией взаимодействия карбоната кальция с водой и углекислым газом с образованием растворимого гидрокарбоната:
-
- CaCO3 + H2O + CO2 ⇄ Ca(HCO3)2 ⇄ Ca2+ + 2HCO3−
(равновесие смещается влево или вправо в зависимости от концентрации углекислого газа).
Огромную роль играет биогенная миграция.
В биосфере
Соединения кальция находятся практически во всех животных и растительных тканях (см. ниже). Значительное количество кальция входит в состав живых организмов. Так, гидроксиапатит Ca5(PO4)3OH, или, в другой записи, 3Ca3(PO4)2·Ca(OH)2 — основа костной ткани позвоночных, в том числе и человека; из карбоната кальция CaCO3 состоят раковины и панцири многих беспозвоночных, яичная скорлупа и др. В живых тканях человека и животных 1,4—2 % Ca (по массовой доле); в теле человека массой 70 кг содержание кальция — около 1,7 кг (в основном в составе межклеточного вещества костной ткани).
Главные особенности
В таблице Менделеева элемент помещен во II группу 4 периода главной подгруппы (А), и все без исключения элементы этой группы относятся к щелочноземельным металлам, со всеми соответствующими признаками и свойствами.
В отличие от типичных металлов кальций обладает некоторыми специфическими свойствами. Есть основания предположить, что это неметалл.
При определенных условиях, как было сказано выше, под высоким давлением он утрачивает металлические свойства.
Элемент химически активен, поэтому в природе соединения кальция содержатся в виде солей, главным образом, в составе минералов или отложений земной коры. Также большое количество кальция содержится в морской воде, где его доля составляет около 1 г/л. Тело человека содержит около 1-1,5 кг вещества, причем, большая его часть содержится в костях, обеспечивая их прочность.
Наиболее богаты кальцием осадочные породы:
- мел.
- известняк.
- гипс.
- мрамор.
- доломит.
- апатит.
Все внутрипещерные образования, сталактиты и сталагмиты представляют собой карбонат СаС03. Строение атома позволяет ему активно вступать в реакцию с другими веществами, поэтому количество разнообразных соединений весьма велико.
Элемент является щелочноземельным металлом. поскольку, вступая в реакцию он отдает электроны, то является восстановителем и степень окисления кальция в соединениях +2. У простого элемента степень окисления равна нулю, как и у всех металлов, поскольку у них равномерно распределена электронная плотность. В неорганической химии понятие «степень окисления» часто тождественно понятию «валентность».
[править] Распространение в природе
По распространенности в природе кальций занимает пятое место среди химических элементов (3,6 % массы земной коры). В связи с высокой химической активностью в свободном состоянии он не встречается. Наиболее распространенными его соединениями являются известняк, мел и мрамор, которые имеют одинаковый химический состав CaCO3, но различную кристаллическую структуру.
Кларк кальция в каменных метеоритах 1,4 %, ультраосновных — 0,7 %, основных — 6,72 %, средних — 4,65 %, кислых породах — 1,58 %.
Кальций входит в состав многих минералов. Составная часть известняков, мрамора и тому подобное. Эти минералы часто образуют целые горные массивы. В больших количествах встречаются также апатиты и фосфориты, основой которых является фосфат кальция Са3(РО4)2. Достаточно распространенным является минерал гипс CaSO4 · 2Н2О.
Кроме того, значительные количества соединений кальция содержатся в почве и природных водах, а также входят в состав животных и растительных организмов. Так, например, минеральная масса костей и зубов животных содержит около 80 % фосфата кальция Са3(РО4)2, а скорлупа яиц почти полностью состоит из карбоната кальция СаСО3.
Химические свойства гидроксида кальция. Химические реакции гидроксида кальция:
Гидроксид кальция является основным основанием, т. е. обладает основными свойствами.
Гидроксид кальция – сильное малорастворимое основание.
Химические свойства гидроксида кальция аналогичны свойствам гидроксидов других основных металлов. Поэтому для него характерны следующие химические реакции:
1. реакция гидроксида кальция и оксида кремния:
SiO2 + Ca(OH)2 → CaSiO3 + H2O (t°).
В результате реакции образуются метасиликат кальция и вода. Реакция происходит при сплавлении реакционной смеси.
2. реакция гидроксида кальция и оксида углерода (II):
Ca(OH)2 + CO → CaCO3 + H2 (t = 400 °C).
В результате реакции образуются карбонат кальция и водород.
3. реакция гидроксида кальция и оксида углерода (IV):
Ca(OH)2 + CO2 → CaCO3 + H2O.
В результате реакции образуются карбонат кальция и вода.
4. реакция гидроксида кальция и оксида серы (IV):
Ca(OH)2 + 2SO2 → Ca(HSO3)2,
Ca(OH)2 + SO2 → CaSO3 + H2O (t°).
В результате реакции образуются в первом случае – гидросульфит кальция, во втором – сульфит кальция и вода. Гидроксид кальция в ходе первой реакции используется в виде суспензии. В ходе второй реакции диоксид серы пропускается через суспензию гидроксида кальция. Вторая реакция протекает при кипении.
5. реакция гидроксида кальция и оксида серы (VI):
Ca(OH)2 + SO3 → CaSO4 + H2O.
В результате реакции образуются сульфат кальция и вода.
6. реакция гидроксида кальция и оксида молибдена:
Ca(OH)2 + MoO2 → CaMoO3 + H2O (t°).
В результате реакции образуются молибдат кальция и вода.
7. реакция гидроксида кальция и гидроксида алюминия:
Ca(OH)2 + 2Al(OH)3 → Ca[Al(OH)4]2.
В результате реакции образуется тетрагидроксоалюминат кальция.
8. реакция гидроксида кальция и угольной кислоты:
H2CO3 + Ca(OH)2 → CaCO3 + 2H2O.
В результате реакции образуются карбонат кальция и вода.
9. реакция гидроксида кальция и ортофосфорной кислоты:
Ca(OH)2 + H3PO4 → CaHPO4 + 2H2O.
В результате реакции образуются гидроортофосфат кальция и вода. В ходе реакции используется концентрированная ортофосфорная кислота.
10. реакция гидроксида кальция с азотной кислотой:
Ca(OH)2 + 2HNO3 → Ca(NO3)2 + 2H2O.
В результате реакции образуются нитрат кальция и вода.
Аналогично проходят реакции гидроксида кальция и с другими кислотами.
11. реакция гидроксида кальция и фтороводорода:
Ca(OH)2 + 2HF → CaF2 + 2H2O.
В результате реакции образуются фторид кальция и вода.
12. реакция гидроксида кальция и бромоводорода:
Ca(OH)2 + 2HBr → CaBr2 + 2H2O.
В результате реакции образуются бромид кальция и вода.
13. реакция гидроксида кальция и йодоводорода:
Ca(OH)2 + 2HI → CaI2 + 2H2O.
В результате реакции образуются йодид кальция и вода.
14. реакция гидроксида кальция и пероксида водорода:
Ca(OH)2 + H2O2 → CaO2 + 2H2O (t = 40-50 °C).
В результате реакции образуются пероксид кальция и вода.
15. реакция гидроксида кальция и сульфата магния:
MgSO4 + Ca(OH)2 → Mg(OH)2 + CaSO4.
В результате реакции образуются гидроксид магния и сульфат кальция. Данная реакция представляет собой химический метод смягчения воды.
16. реакция гидроксида кальция и хлорида магния:
MgCl2 + Ca(OH)2 → Mg(OH)2 + CaCl2.
В результате реакции образуются гидроксид магния и хлорид кальция. В ходе реакции используется насыщенный раствор гидроксида кальция.
17. реакция гидроксида кальция и карбоната натрия:
Na2CO3 + Ca(OH)2 → CaCO3 + 2NaOH.
В результате реакции образуются гидроксид натрия и карбонат кальция. Равновесие реакции смещено в сторону образования NaOH за счет плохой растворимости CaCO3. Данная реакция именуется также каустификацией соды и представляет собой метод получения гидроксида натрия.
18. реакция гидроксида кальция и карбоната калия:
K2CO3 + Ca(OH)2 → CaCO3 + 2KOH (t°).
В результате реакции образуются гидроксид калия и карбонат кальция. В ходе реакции используется насыщенный раствор гидроксида кальция. Реакция протекает при кипячении карбоната калия в известковом молоке.
19. реакция гидроксида кальция и карбоната лития:
Li2CO3 + Ca(OH)2 → 2LiOH + CaCO3 (t < 600 °C)
В результате реакции образуются гидроксид лития и карбонат кальция.
20. реакция гидроксида кальция и карбоната магния:
MgCO3 + Ca(OH)2 → Mg(OH)2 + CaCO3.
В результате реакции образуются гидроксид магния и карбонат кальция.
21. реакция гидроксида кальция и сульфита натрия:
Na2SO3 + Ca(OH)2 → 2NaOH + CaSO3.
В результате реакции образуются гидроксид натрия и сульфит кальция.
22. реакция термического разложения гидроксида кальция:
Ca(OH)2 → CaO + H2O (t = 580 °C).
В результате реакции образуются оксид кальция и вода.
Применение и состав сплавов кальция
Кальций легко взаимодействует с кислородом, серой, азотом, водородом и многими другими элементами и при высоких температурах восстанавливает оксиды большинства металлов, поэтому его применяют для раскисления и десульфурации расплавленных металлов. Однако высокая стоимость и сложность хранения и использования металлического кальция ограничили применение его в промышленном масштабе в черной металлургии. Соединения кальция с кремнием — силициды кальция, значительно дешевле и более устойчивы при нормальной температуре. В связи с этим для раскисления, десульфурации и дегазации стали и литейного чугуна, для регулирования размера и формы неметаллических включений в стали, для графитизации и получения однородного серого чугуна используют силикокальций — сплав кальция с кремнием или тройной сплав кальция, кремния и железа, который обладает повышенной плотностью и кальций которого лучше усваивается жидкой сталью. Кроме того, силикокальций марок СК10 и СК15 является основой для производства многих комплексных раскислителей и модификаторов. Некоторое количество силикокальция используют в пиротехнике, для получения некоторых чистых металлов кальцийсиликотермическим методом и т. д.
Химический состав сплавов кальция по стандартам ряда стран приведен в табл. 27. Силикокальций марок СК25 и СК30 содержит 2—4 % SiC и более, 3 O2, 36—210 см3 Н2 и до 70 см3 N2 на 100 г сплава. Содержание серы в них колеблется в пределах 0,05—0,08% и может достигать 0,13—0,20%. В СК10 и СК15, полученном углеродотермическим способом, содержится св 9,09; CaSi2 81,5; Fe2Si5 4,65; Ca2Si3Al44,23, примесей 0,33.
Силикотермический силикокальций марок СК10 и СК15, производство которого освоено в СССР в последние годы, значительно более чист по содержанию вредных примесей. В пересчете на сплав с 30 % Са он содержит примерно по 0,016 %S и Р, 0,08% С, тогда как для силикокальция марок СК25 и СК30 характерно 0,08 % S, 0,02 % Р и 1,15 % С. Расход силикокальция обычно колеблется в пределах 2—4 кг/т стали.
Металлы, неметаллы, металлоиды
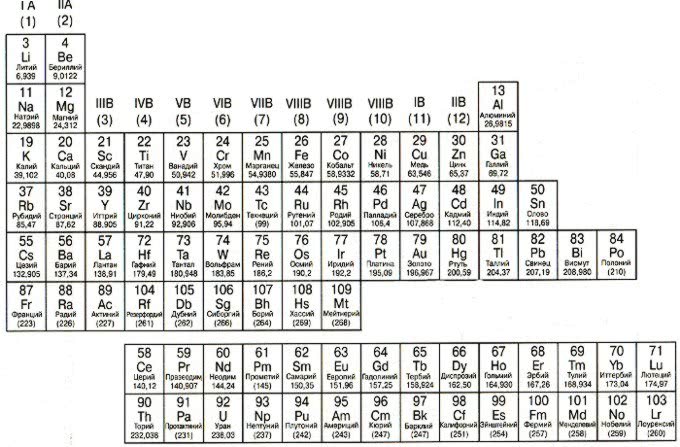
Расположены в Периодической таблице слева от ступенчатой диагональной линии, которая начинается с Бора (В) и заканчивается полонием (Po) (исключение составляют германий (Ge) и сурьма (Sb). Нетрудно заметить, что металлы занимают бОльшую часть Периодической таблицы. Основные свойства металлов: твердые (кроме ртути); блестят; хорошие электро- и теплопроводники; пластичные; ковкие; легко отдают электроны.
Элементы, расположенные справа от ступенчатой диагонали B-Po, называются неметаллами
. Свойства неметаллов прямо противоположны свойствам металлов: плохие проводники тепла и электричества; хрупкие; нековкие; непластичные; обычно принимают электроны.
Металлоиды
Между металлами и неметаллами находятся полуметаллы
(металлоиды). Для них характерны свойства как металлов, так и неметаллов. Основное применение в промышленности полуметаллы нашли в производстве полупроводников, без которых немыслима ни одна современная микросхема или микропроцессор.






