Физиологическая роль олова в организме.
Информация о физиологической роли олова в организме человека и животных противоречива. Олово образует больше количество металлоорганических соединений (т.е. соединений, в которых есть хотя бы одна связь Sn-C). К ним относятся тетраалкильные соединения R4Sn, алкилгалогеноводороды R3SnГ, R2SnГ2, RSnГ3, гидроксиды R3SnOH и другие кислородосодержащие соединения, сульфиды R2SnS. В организме олово находится в основном в виде жирорастворимых соединений.
В человеческом теле диспергировано до 0,0002% олова, обычно же — на порядок меньше. По этой причине для человека оно относится к примесным микроэлементам. Ежедневно человек «съедает» 0,02-17 мг олова, особенно при активном потреблении консервов, хранящихся в банках из луженой жести. В кровь олово практически не всасывается, т.к. в результате гидролиза образуются гидроксиды или другие труднорастворимые неорганические соединения. Поступление его в кровь ограничивается значениями 0,02-0,2 мг в сутки (в виде белковых комплексов). Однако, это количество олова быстро распределяется по разным органам. Олово депонируется в скелете (10 мкммоль/кг), печени (2,7), легких (2,4), почках (1,6), коже (1,3). Оно входит в состав желудочного гормона гастрина. Этот гормон регулирует выработку соляной кислоты в желудке и увеличивает секрецию пепсина (пищеварительный фермент, расщепляющий белки).
В опытах на крысах было показано, что малые дозы соединений олова способствуют их росту.
Потребность в олове обычно удовлетворяется обычным питанием. Дефицит наступает при длительном его потреблении менее 1 мг в день. Испытания на лабораторных животных показали, что при нехватке олова замедлялся рост и привес у некоторых видов, нарушался минеральный состав внутренних органов, развивалась алопеция, ухудшался слух.
Вы здесь
Изотопы олова
Природное олово состоит из десяти стабильных изотопов: 112Sn (олово-112), 114Sn (олово-114), 115Sn (олово-115), 116Sn (олово-116), 117Sn (олово-117), 118Sn (олово-118), 119Sn (олово-119), 120Sn (олово-120), 122Sn (олово-122) и 124Sn (олово-124).
Для некоторых из них энергетически возможен двойной бета-распад, однако экспериментально он пока (по данным на 2018 г.) не наблюдался, поскольку предсказываемый период полураспада очень велик (более 1020 лет).
| ИЗОТОП |
ПРИРОДНОЕ СОДЕРЖАНИЕ, % |
СТЕПЕНЬ ОБОГАЩЕНИЯ, % |
ХИМИЧЕСКАЯ ФОРМА |
| 112Sn | 0,97 | 99,90 |
металл (Sn) |
| 114Sn | 0,66 | 98,00 | |
| 115Sn | 0,34 | 90,00 | |
| 116Sn | 14,54 | 99,50 | |
| 117Sn | 7,68 | 90,00 | |
| 118Sn | 24,22 | 98,50 | |
| 119Sn | 8,59 | 87,00 | |
| 120Sn | 32,58 | 99,00 | |
| 122Sn | 4,63 | 99,00 | |
| 124Sn | 5,79 | 99,90 |
Основные сферы использования: научные исследования, материаловедение, медицина, лазерная техника, метрология, металлургия.
| По данным открытых источников | |
| ИЗОТОП | ОБЛАСТИ ПРИМЕНЕНИЯ |
| 112Sn |
— производство радиоизотопа 113mIn (индий-113m) для использования в медицине, диагностики заболеваний сердца, лёгких, сосудов мозга, печени и пр.; — получение радиоизотопа 113Sn (олово-113) для изготовления источников моноэнергетических электронов для калибровки детекторов электронов |
| 114Sn | — ядерно-физические исследования |
| 115Sn | — изучение структуры фторидов олова методом ядерного магнитного резонанса (ЯМР) в твёрдом теле. |
| 116Sn |
— изучение распределения примесей в технологии получения галлия; — получение радиоизотопа 117mSn, который используется в науке для изучения эффекта Мёссбауэра и в медицине для диагностики рака кости |
| 117Sn |
— проведение химических исследований; — получение медицинского радиоизотопа 117mSn, который используется в диагностике рака кости |
| 118Sn | — изготовление мёссбауэровского источника на основе 119mSn для разработки резонансных детекторов гамма-излучения с целью повышения эффективности использования метода ядерного гамма-резонанса (ЯГР) для проведения фазового анализа веществ и измерения параметров механических колебаний |
| 119Sn |
— метрологическое обеспечение ЯГР-измерений; — разработка резонансных детекторов гамма-излучения для повышения эффективности использования метода ЯГР; — изучение сплавов в металлургии, коррозии циркониевых сплавов; исследование служебных характеристик металлов методом ЯГР; — изучение катализаторов и процесса ионного обмена методом ЯГР; — изучение свойств магнитных полупроводников методом ЯГР; — исследование сверхпроводимости посредством резонансной гамма-спектрометрии; — исследование промышленно важных катализаторов нефтехимической промышленности методами ЯГР и ЯМР |
| 120Sn | — исследования сверхпроводимости |
| 122Sn | — получение радиоизотопа 123Sn (олово-123) для физических и химических измерений методом ЯГР |
| 124Sn |
— изучение двойного β-распада; |
| Изотопы олова 117Sn и 119Sn являются мёссбауэровскими изотопами и применяются в гамма-резонансной спектроскопии. |
По вопросам приобретения обращаться к специалистам отдела продаж:Варлакова Мария Владимировна
Тел. +7 (39169) 9-49-11Добровольский Алексей Владимирович
Тел. +7 (39169) 9-49-03Рябченко Оксана Сергеевна
Тел. +7 (39169) 9-31-73
Эл. почта: market.ecp@rosatom.ru, market@ecp.ru
Преимущества и недостатки олова
Данный металл практически не используется в строительстве, поскольку не отличается высокой механической прочностью. В основном в настоящее время используют не чистый металл, а его сплавы.
Выделим основные преимущества данного металла. Особое значение имеет ковкость, ее используют в процессе изготовления предметов быта. Например, эстетично выглядят подставки, светильники, выполненные из данного металла.
Оловянное покрытие позволяет существенно снижать трение, благодаря чему изделие защищено от преждевременного износа.
Среди основных недостатков данного метала можно упомянуть его незначительную прочность. Олово непригодно для изготовления частей и деталей, предполагающих существенные нагрузки.

История
Олово было известно человеку уже в IV тысячелетии до н. э. Этот металл был малодоступен и дорог, поэтому изделия из него редко встречаются среди римских и греческих древностей. Об олове есть упоминания в Библии, Четвёртой Книге Моисея. Олово является (наряду с медью) одним из компонентов оловяннистой бронзы, изобретённой в конце или середине III тысячелетия до н. э. Поскольку бронза являлась наиболее прочным из известных в то время металлов и сплавов, олово было «стратегическим металлом» в течение всего «бронзового века», более 2000 лет (очень приблизительно: XXXV—XI века до н. э.).
Чистое олово получено не ранее XII в., о нем упоминает в своих трудах Р. Бэкон. До этого олово всегда содержало переменное количество свинца. Хлорид SnCl4 впервые получил А. Либавий в 1597 г. Аллотропию олова и явление «оловянной чумы» объяснил Э. Кохен в 1899 г.
Расплавленное олово
ЗАПАСЫ И ДОБЫЧА
 Олово — редкий рассеянный элемент, по распространенности в земной коре олово занимает 47-е место. Кларковое содержание олова в земной коре составляет, по разным данным, от 2·10−4 до 8·10−3 % по массе. Основной минерал олова — касситерит (оловянный камень) SnO2, содержащий до 78,8 % олова. Гораздо реже в природе встречается станнин (оловянный колчедан) — Cu2FeSnS4 (27,5 % Sn). Мировые месторождения олова находятся в основном в Китае и Юго-Восточной Азии — Индонезии, Малайзии и Таиланде. Также есть крупные месторождения в Южной Америке (Боливии, Перу, Бразилии) и Австралии.
Олово — редкий рассеянный элемент, по распространенности в земной коре олово занимает 47-е место. Кларковое содержание олова в земной коре составляет, по разным данным, от 2·10−4 до 8·10−3 % по массе. Основной минерал олова — касситерит (оловянный камень) SnO2, содержащий до 78,8 % олова. Гораздо реже в природе встречается станнин (оловянный колчедан) — Cu2FeSnS4 (27,5 % Sn). Мировые месторождения олова находятся в основном в Китае и Юго-Восточной Азии — Индонезии, Малайзии и Таиланде. Также есть крупные месторождения в Южной Америке (Боливии, Перу, Бразилии) и Австралии.
В России запасы оловянных руд расположены в Чукотском автономном округе (Пыркакайские штокверки; рудник/посёлок Валькумей, Иультин — разработка месторождений закрыта в начале 1990-х годов), в Приморском крае (Кавалеровский район), в Хабаровском крае (Солнечный район, Верхнебуреинский район (Правоурмийское месторождение)), в Якутии (месторождение Депутатское) и других районах.
В процессе производства рудоносная порода (касситерит) подвергается дроблению до размеров частиц в среднем ~ 10 мм, в промышленных мельницах, после чего касситерит за счет своей относительно высокой плотности и массы отделяется от пустой породы вибрационно-гравитационным методом на обогатительных столах. В дополнение применяется флотационный метод обогащения/очистки руды. Таким образом удается повысить содержание олова в руде до 40-70 %. Далее проводят обжиг концентрата в кислороде для удаления примесей серы и мышьяка. Полученный концентрат оловянной руды выплавляется в печах. В процессе выплавки восстанавливается до свободного состояния посредством применения в восстановлении древесного угля, слои которого укладываются поочередно со слоями руды, или алюминием (цинком) в электропечах: SnO2 + C = Sn + CO2. Особо чистое олово полупроводниковой чистоты готовят электрохимическим рафинированием или методом зонной плавки.
Кристаллическая решётка олова:
| 500 | Кристаллическая решётка | |
| 511 | Кристаллическая решётка #1 | β-олово (белое олово) |
| 512 | Структура решётки |
Тетрагональная объёмно-центрированная |
| 513 | Параметры решётки | a = 5,8197 Å, c = 3,175 Å |
| 514 | Отношение c/a | 0,546 |
| 515 | Температура Дебая | 170 K |
| 516 | Название пространственной группы симметрии | I41/amd |
| 517 | Номер пространственной группы симметрии | 141 |
| 521 | Кристаллическая решётка #2 | α-олово (серое олово) |
| 522 | Структура решётки |
Кубическая алмазная |
| 523 | Параметры решётки | a = 6,46 Å |
| 524 | Отношение c/a | |
| 525 | Температура Дебая | |
| 526 | Название пространственной группы симметрии | Fd_ 3m |
| 527 | Номер пространственной группы симметрии | 225 |
Класс холодильника: основные типы
Существуют разные климатические классы, они определяют температурные показатели и влажность, в которых будет работать холодильник. Изучим основные климатические классы холодильников. Всего существует 4 основных климат-класса, с которыми вы, скорее всего, столкнетесь в своем оборудовании. Они включают:
1.Климатический класс N. Он предназначен для оборудования, которое способно работать в нормальном диапазоне температур, а точнее – от + 16C до + 32C. Этот климатический класс поддерживает высокий уровень энергосбережения холодильников. Они потребляют небольшое количество электроэнергии и более популярны для использования в бытовых условиях.
2.Климатический класс Т. Он предназначен для холодильников, которые могут работать в тропических (сухих) зонах с температурой от + 18C до + 43C. В таких холодильниках, вы обнаружите, скорее всего, много теплоизоляции. Это означает, что стены будут толще, чтобы они могли должным образом поддерживать низкие оптимальные температуры. Кроме того, они обычно имеют мощный и высокопроизводительный компрессор и с большей вероятностью будут использовать стабильные элементы для предотвращения образования грибка, плесени и прочих процессов развития микроорганизмов, которые влияют на качество продуктов. С большой вероятностью такие холодильники можно найти на коммерческой кухне.
3.Климатический класс sn. Такие холодильники подходят для субнормального климата с температурой от + 10C до + 32C. Холодильники с таким классом лучше приспособлены для работы в более холодных помещениях или местах с более низкими температурами, чем обычно. Эта характеристика делает такой агрегат идеальным для размещения в подвале. Этот вид холодильников чаще всего используется в промышленных процессах.
4.Климатический класс st. Этот класс обозначает холодильники, которые работают в субтропическом климате. Обычно это места с жарким и влажным климатом. Они могут работать при температуре от + 18С до + 38С. Для холодных регионов не подходят.
Учитывая различные климатические условия по всему миру и тот факт, что в некоторых регионах наблюдается более широкий температурный диапазон, иногда трудно выбрать холодильник определенного климатического класса.
Большинство производителей должны учитывать это, поэтому возникла потребность в разработке холодильного оборудования, отвечающего различным климатическим классам, как по экономическим причинам, так и по причинам эффективности. Эти классы включают:
1.Климатический класс n-st. Этот класс обозначает холодильники, которые работают при температуре окружающей среды от + 16C до + 38C.
2.Климатический класс NT. Температурный диапазон таких моделей холодильников от + 16С до + 43С.
3.Климатический класс sn-t. Эта маркировка чаще всего встречается на универсальных холодильниках, которые можно использовать в любом климате. Климатический класс sn t включает в себя холодильники, которые могут работать при температуре окружающей среды от + 10С до + 43С.
4.Климатический класс SN-ST. Обычно это назначается холодильникам, которые могут работать в субнормальном и субтропическом климате. Они могут легко работать при температуре окружающей среды от + 10С до + 38С.
В коммерческом холодильном оборудовании климатическим классам также присваиваются номера, причем каждый номер предназначен для обозначения условий окружающей температуры и относительной влажности (RH), в которых может работать холодильник или морозильная камера. Это помогает владельцам бизнеса сделать правильный выбор в зависимости от их коммерческих кухонь, где максимально сохранение продуктов необходимо всегда. Классы делятся на три, а именно:
·Климатический класс 3 — этот холодильник может работать при максимальной температуре окружающей среды 25C и относительной влажности 60%.
·Климатический класс 4 — этот холодильник может работать при максимальной температуре окружающей среды 30C и относительной влажности 55%.
·Климатический класс 5 — этот холодильник может работать при максимальной температуре окружающей среды 40C и относительной влажности 40%.
Главный совет: если у вас загруженная кухня, где ингредиенты и продукты питания нужно хранить, но держать под рукой для эффективности, всегда выбирайте холодильник или морозильник с климатическим классом 4 или выше.
Соединения.
Олово образует различные химические соединения, многие из которых находят важное промышленное применение. Кроме многочисленных неорганических соединений, атом олова способен к образованию химической связи с углеродом, что позволяет получать металлоорганические соединения, известные как оловоорганические (см
также МЕТАЛЛООРГАНИЧЕСКИЕ СОЕДИНЕНИЯ). Водные растворы хлоридов, сульфатов и фтороборатов олова служат электролитами для осаждения олова и его сплавов. Оксид олова применяют в составе глазури для керамики; он придает глазури непрозрачность и служит красящим пигментом. Оксид олова можно также осаждать из растворов в виде тонкой пленки на различных изделиях, что придает прочность стеклянным изделиям (или уменьшает вес сосудов, сохраняя их прочность). Введение станната цинка и других производных олова в пластические и синтетические материалы уменьшает их возгораемость и препятствует образованию токсичного дыма, и эта область применения становится важнейшей для соединений олова. Огромное количество оловоорганических соединений расходуется в качестве стабилизаторов поливинилхлорида – вещества, используемого для изготовления тары, трубопроводов, прозрачного кровельного материала, оконных рам, водостоков и др. Другие оловоорганические соединения используются как сельскохозяйственные химикаты, для изготовления красок и консервации древесины.
Система классификации
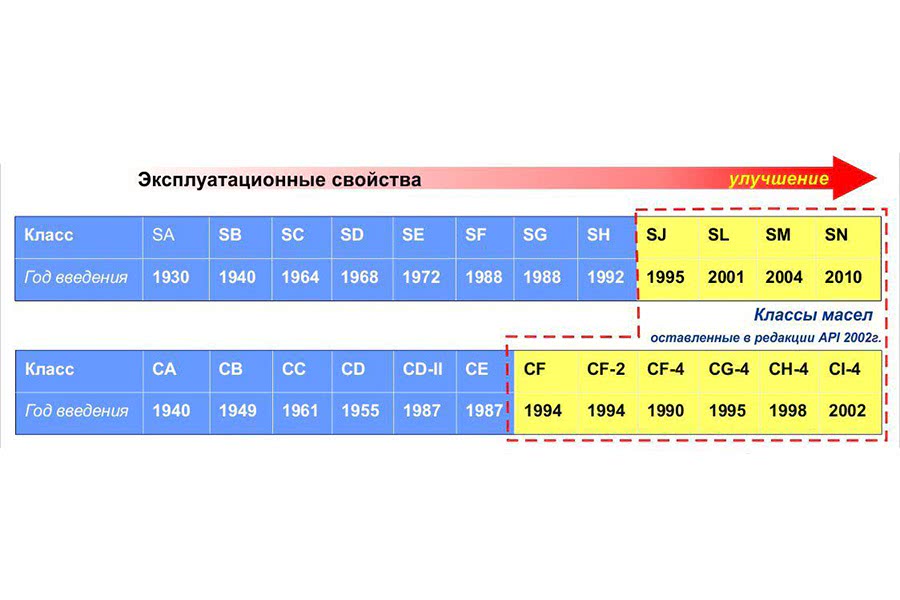
Американский институт топлива (api) – это учреждение, которое занимается классифицированием масел, определением минимального перечня требований к ним, выдачей соответствующих сертификатов производителям данной продукции.
Классификация api включает в себя обозначения «S», «C» и «EC» с последующими цифровыми и буквенными обозначениями. Расшифровка символа «S» указывает на продукт, пригодный для применения в бензиновом двигателе, а «C» — в дизельном. Допуск «EC» присваивается энергосберегающим маслам, область применения которых пока ограничена бензиновыми моторами.
К каждому из указанных символов добавляются латинские буквы в алфавитном порядке. Чем дальше буква от начала алфавита, тем более высоким классом отличается продукт. Например, стандарт api sn был введен в 2010 году и на данный момент является самым высоким среди классификации масел для бензиновых двигателей.
Применение
Сурьма всё больше применяется в полупроводниковой промышленности при производстве диодов, инфракрасных детекторов, устройств с эффектом Холла. Является компонентом свинцовых сплавов, увеличивающим их твёрдость и механическую прочность. Область применения включает:
- батареи;
- антифрикционные сплавы;
- типографские сплавы;
- стрелковое оружие и трассирующие пули;
- оболочки кабелей;
- спички;
- лекарства, противопротозойные средства;
- пайка — некоторые бессвинцовые припои содержат 5 % Sb;
- использование в линотипных печатных машинах.
Вместе с оловом и медью сурьма образует металлический сплав — баббит, обладающий антифрикционными свойствами и использующийся в подшипниках скольжения. Также Sb добавляется к металлам, предназначенным для тонких отливок.
Соединения сурьмы в форме оксидов, сульфидов, антимоната натрия и трихлорида сурьмы, применяются в производстве огнеупорных соединений, керамических эмалей, стекла, красок и керамических изделий. Триоксид сурьмы является наиболее важным из соединений сурьмы и главным образом используется в огнестойких композициях. Сульфид сурьмы является одним из ингредиентов в спичечных головках.
Природный сульфид сурьмы, стибнит, использовали в библейские времена в медицине и косметике. Стибнит до сих пор используется в некоторых развивающихся странах в качестве лекарства.
Соединения сурьмы, например, меглюмина антимониат (глюкантим) и натрия стибоглюконат (пентостам), применяются в лечении лейшманиоза.
Электроника
Входит в состав некоторых припоев. Также может использоваться в качестве легирующей примеси к полупроводникам (донор электронов для кремния и германия).
Термоэлектрические материалы
Теллурид сурьмы применяется как компонент термоэлектрических сплавов (термо-ЭДС 150—220 мкВ/К) с теллуридом висмута.
Применение
Металл имеется в продаже на многих металлургических заводах и компаниях. Выпускается в виде чушек, прутков, проволоки, цилиндров, анодов, изготовленных из чистого простого вещества, такого как олово. Цена колеблется от 900 до 3000 рублей за кг.
Олово в чистом виде применяется редко. В основном используются его сплавы и соединения – соли. Олово для пайки применяется в случае скрепления деталей, которые не подвергаются воздействию высоких температур и сильных механических нагрузок, выполненных из медных сплавов, стали, меди, но не рекомендуется для изготовленных из алюминия или его сплавов. Свойства и характеристики оловянных сплавов описаны в соответствующем разделе.
Припои используют для пайки микросхем, в этой ситуации также идеально подходят сплавы на основе такого металла, как олово. Фото изображает процесс применения оловянно-свинцового сплава. С помощью него можно выполнить достаточно тонкие работы.
Ввиду высокой стойкости олова к коррозии его применяют для изготовления луженого железа (белой жести) – жестяных банок для пищевых продуктов. В медицине, в частности в стоматологии, олово задействовано для выполнения пломбирования зубов. Оловом покрыты домовые трубопроводы, из его сплавов изготовлены подшипники. Неоценимо важен вклад данного вещества и в электротехнику.

Водные растворы таких солей олова, как фторбораты, сульфаты, а также хлориды, используют в качестве электролитов. Оксид олова – это глазурь для керамики. Путём введения в пластические и синтетические материалы различных производных олова представляется возможным уменьшить их возгораемость и выделение вредоносных дымов.
Физические свойства.
Олово – мягкий серебристо-белый пластичный металл (может быть прокатан в очень тонкую фольгу – станиоль) с невысокой температурой плавления (легко выплавляется из руд), но высокой температурой кипения. Олово имеет две аллотропные модификации: a-Sn (серое олово) с гранецентрированной кубической кристаллической решеткой и b-Sn (обычное белое олово) с объемноцентрированной тетрагональной кристаллической решеткой. Фазовый переход b a ускоряется при низких температурах (–30° С) и в присутствии зародышей кристаллов серого олова; известны случаи, когда оловянные изделия на морозе рассыпались в серый порошок («оловянная чума»), но это превращение даже при очень низких температурах резко тормозится наличием мельчайших примесей и поэтому редко встречается, представляя скорее научный, чем практический интерес. См. также АЛЛОТРОПИЯ; ЭЛЕМЕНТЫ ХИМИЧЕСКИЕ; ПЕРИОДИЧЕСКАЯ СИСТЕМА ЭЛЕМЕНТОВ.
Чистое олово обладает низкой механической прочностью при комнатной температуре (можно согнуть оловянную палочку, при этом слышится характерный треск, обусловленный трением отдельных кристаллов друг о друга) и поэтому редко используется. Однако оно легко образует сплавы с большинством других черных и цветных металлов. Оловосодержащие сплавы обладают прекрасными антифрикционными свойствами в присутствии смазки, поэтому широко используются как материал подшипников.
Периодическая таблица
Горизонтальные ряды таблицы называются периодами. Все элементы, относящиеся к одному периоду, имеют одинаковое число электронных оболочек. У элементов 2-го периода две оболочки, у элементов 3-го периода три и так далее. Восемь вертикальных рядов называются группами, с отдельным блоком переходных металлов между 2-й и 3-й группами. У элементов с атомными номерами меньше 20 (за исключением переходных металлов) номер группы совпадает с числом электронов на внешнем уровне. Регулярное изменение свойств элементов одного периода объясняется изменением числа электронов. Так во 2-м периоде температура плавления твердых элементов постепенно возрастает от лития к углероду. Все элементы одной группы имеют сходные химические свойства . Некоторые группы имеют особые названия . Так, группу 1 составляют щелочные металлы, группу 2 — щелочноземельные. Элементы группы 7 называются галогенами, элементы группы 8 — благородными газами. На рисунке вы видите халькопирит, в котором содержится медь, железо и сера.
Все мы знаем, что водород наполняет нашу Вселенную на 75%. Но знаете ли вы, какие еще есть химические элементы, не менее важные для нашего существования и играющие значительную роль для жизни людей, животных, растений и всей нашей Земли? Элементы из этого рейтинга формируют всю нашу Вселенную!
Сера (распространенность относительно кремния – 0.38)
Этот химический элемент в таблице Менделеева значится под символом S и характеризуется атомным номером 16. Сера очень распространена в природе.
Железо (распространенность относительно кремния – 0.6)
Обозначается символом Fe, атомный номер – 26. Железо очень часто встречается в природе, особенно важную роль оно играет в формировании внутренней и внешней оболочки ядра Земли.
Магний (распространенность относительно кремния – 0.91)
В таблице Менделеева магний можно найти под символом Mg, и его атомный номер – 12. Что самое удивительное в этом химическом элементе, так это то, что он чаще всего выделяется при взрыве звезд в процессе их преобразования в сверхновые тела.Кремний (распространенность относительно кремния – 1)
Обозначается как Si. Атомный номер кремния – 14. Этот серо-голубой металлоид очень редко встречается в земной коре в чистом виде, но довольно распространен в составе других веществ. Например, его можно обнаружить даже в растениях.
Углерод (распространенность относительно кремния – 3.5)
Углерод в таблице химических элементов Менделеева значится под символом С, его атомный номер – 6. Самой знаменитой аллотропной модификацией углерода являются одни из самых желанных драгоценных камней в мире – алмазы. Углерод активно применяют и в других в промышленных целях более будничного назначения. Азот (распространенность относительно кремния – 6.6)
Символ N, атомный номер 7. Впервые открытый шотландским врачом Дэниелом Рутерфордом (Daniel Rutherford), азот чаще всего встречается в форме азотной кислоты и нитратов.Неон (распространенность относительно кремния – 8.6)
Обозначается символом Ne, атомный номер — 10. Не секрет, что именно этот химический элемент ассоциируется с красивым свечением. Кислород (распространенность относительно кремния – 22)
Химический элемент под символом О и с атомным номером 8, кислород незаменим для нашего существования! Но это не значит, что он присутствует только на Земле и служит только для человеческих легких. Вселенная полна сюрпризов. Гелий (распространенность относительно кремния – 3.100)
Символ гелия – He, атомный номер – 2. Он бесцветен, не имеет запаха и вкуса, не ядовит, и его точка кипения – самая низкая среди всех химических элементов. А еще благодаря ему шарики взмывают ввысь!
Водород (распространенность относительно кремния – 40.000)
Истинный номер один в нашем списке, водород находится в таблице Менделеева под символом Н и обладает атомным номером 1. Это самый легкий химический элемент периодической таблицы и самый распространенный элемент во всей изученной человеком Вселенной.
Есть наиболее распространённый химический элемент и наиболее распространённое вещество на нашей удивительной планете, а есть самый распространённый химический элемент на просторах Вселенной.
Происхождение названия
Латинское название stannum, связанное с санскритским словом, означающим «стойкий, прочный», первоначально относилось к сплаву свинца и серебра, а позднее к другому, имитирующему его сплаву, содержащему около 67 % олова; к IV веку н. э. этим словом стали называть собственно олово.
Слово олово — общеславянское, однако в некоторых славянских языках такое же или однокоренное слово (польск. ołów, чеш. olovo, серб. олово и др.) используется для обозначения другого, внешне похожего металла — свинца. Слово олово имеет соответствия в балтийских языках (ср. лит. alavas, alvas, латыш. alva — «олово», прусск. alwis — «свинец»). Оно является суффиксальным образованием от корня ol- (ср. древневерхненемецкое elo — «жёлтый», лат. albus — «белый» и пр.), так что металл назван по цвету.
Биологическая роль и воздействие на организм
Сурьма токсична. Относится к микроэлементам. Её содержание в организме человека составляет 10−6 % по массе. Постоянно присутствует в живых организмах, физиологическая и биохимическая роль не выяснена. Сурьма проявляет раздражающее и кумулятивное действие. Накапливается в щитовидной железе, угнетает её функцию и вызывает эндемический зоб. Однако, попадая в желудочно-кишечный тракт, соединения сурьмы не вызывают отравления, так как соли Sb(III) там гидролизуются с образованием малорастворимых продуктов. При этом соединения сурьмы (III) более токсичны, чем сурьмы (V). Пыль и пары Sb вызывают носовые кровотечения, сурьмяную «литейную лихорадку», пневмосклероз, поражают кожу, нарушают половые функции. Порог восприятия привкуса в воде — 0,5 мг/л. Смертельная доза для взрослого человека — 100 мг, для детей — 49 мг. Для аэрозолей сурьмы ПДК в воздухе рабочей зоны 0,5 мг/м³, в атмосферном воздухе 0,01 мг/м³. ПДК в почве 4,5 мг/кг. В питьевой воде сурьма относится ко 2 классу опасности, имеет ПДК 0,005 мг/л, установленную по санитарно-токсикологическому лимитирующему признаку вредности. В природных водах норматив содержания составляет 0,05 мг/л. В сточных промышленных водах, сбрасываемых на очистные сооружения, имеющие биофильтры, содержание сурьмы не должно превышать 0,2 мг/л.
Какие климатические классы холодильников бывают
Стандартом установлены четыре климатических класса для холодильного оборудования, каждый и которых имеет свою маркировку и температурные диапазоны:
- N– нормальный;
- SN – субнормальный;
- ST – субтропический;
- T – тропический.
Из-за изменений температурных условий многие компании стали выпускать холодильные установки с двойной маркировкой:
- N-ST – сочетание характеристик нормального и субтропического климатических классов;
- N-T – нормальный + тропический;
- SN-ST – субнормальный + субтропический;
- SN-T – субнормальный + тропический.
Подобные смешанные модели охватывают значительно больший температурный диапазон, что делает их более универсальными.
Характеристика климатических классов
В таблице представлены стандартные климатические классы, их краткая характеристика и популярные производители таких моделей.
| Название климатического класса | Допустимый диапазон температурных значений | Характеристики | Производители |
| N (нормальный) | +16…+32°С | Универсальный вид, который чаще всего устанавливается в жилых домах. Подходит для умеренного климата без длительных холодных и жарких периодов.
Отличается оптимальным энергопотреблением и демократичной ценой |
Nord, Indesit, LG |
| SN (субнормальный) | +10…+32°С | Оборудование подходит для помещений с нестабильным отоплением (холодные коридоры, кладовки). Чаще всего используется на небольших производствах | Samsung, Bosch |
| ST (субтропический) | +18…+38°С | Техника предназначена для жаркого климата с повышенной влажностью. Приборы устойчивы к сезонным температурным скачкам, но не подходят для работы в холодных помещениях | Samsung, Sharp, Electrolux |
| T (тропический) | +18…+43°С | Модели предназначены для регионов с очень жарким и сухим климатом. Нельзя ставить в помещениях с повышенной влажностью.
Отличаются высоким энергопотреблением, большим слоем теплоизоляции и высокой стоимостью. |
Samsung, Panasonic, Whirpool |
Холодильники со смешанными климатическими классами имеют следующие характеристики:
- N-ST – рабочая температура таких устройств составляет +16…+38°С;
- N-T – приспособлен для работы при температурных показателях +16…+43°С;
- SN-ST – функционирует в температурном диапазоне +10…+38°С;
- SN-T – самое универсальное оборудование, которое способно работать при +10…+43°С.
Несмотря на то, что подобное оборудование стоит дороже и потребляет значительно больше электроэнергии, оно приобретает все большую популярность. Это связано с частыми изменениями погоды (аномальная жара, рекордные холода), поздним включением и ранним отключением отопления.
Модели холодильников со смешанными классами представлены ведущими производителями: Samsung, Bosch, Liebherr, Whirpool.
Чем отличаются холодильники с разными климатическими классами
В зависимости от климатического класса каждая модель холодильного оборудования имеет свои особенности в конструкции:
- Мощность компрессора. Приборы, которые используются в жарком климате, оснащаются компрессорами высокой мощности. Это связано с необходимостью в постоянном охлаждении продуктов в отсеках и морозилке холодильника. Для тропического и субтропического классов используют компрессоры с самой высокой производительностью.
- Теплоизоляция. В технике для жаркого климата теплоизоляционный слой больше по сравнению с приборами, используемыми в более прохладных условиях.
- Потребление электроэнергии. При прочих равных показателях агрегаты, работающие в широком температурном диапазоне, потребляют гораздо больше энергоресурсов.
- Материалы. Если модели предназначены для эксплуатации в помещениях с повышенной температурой и влажностью, то они производятся из специальных материалов с покрытием, которое защищает корпус от влаги и плесени.
- Пространство для теплообмена. Техника, предназначенная для работы в жаре, оснащена большей площадью для теплообмена (конденсаторами и испарителями).
Комплектовка моделей соответствующими деталями регламентируется стандартом IEC 62552.
Выплавка
Восстановление происходит путем плавления касситерита с углесодержащими материалами в специализированных печах отражательного или шахтового типа. Шахтные печи принято использовать издавна: в них, чередуя, грузят слоями древесный уголь и касситерит. Отражательные устройства являются более современными и распространенными. Топливом выступает каменный уголь, а руда перемешивается с антрацитом и известняковыми породами.
Результат восстановительных работ — шлаки, обогащенные до 25 % оловом. Полученные материалы подвергают дальнейшей обработке, с последующей переплавкой под более высокими температурными режимами. Весь процесс имеет особый контроль со своей технологией, которая строго соблюдается, во избежание получения слишком больших остатков олова в шлаках после вторичной обработки.
Что означает класс api sn?
Спецификация api sn – это признак того, что перед вами продукт наивысшей категории, отвечающий самым высоким требованиям и стандартам.
В разработке этого класса приняло участие три крупных организации, спецификация которых связана с автомобильной промышленностью и продуктами нефтепереработки. Специалисты этих организаций сконцентрировали усилия на создании инновационного продукта, который бы позволил соответствовать требованиям современного мира.
Так, к обязательным характеристикам разрабатываемого продукта было причислено энергосбережение, соответствие другим классификациям, совместимость с системами нейтрализации выхлопных газов и биотопливом.
Естественно, в основу инновационного продукта вошли предыдущие разработки американского института топлива. Однако при этом были учтены и исключены недостатки этих разработок. Например, защита от износа и антикоррозийный эффект у масел класса api sn значительно выше.






